Eureka:E轮融资4500万美元,华人科学家继续发力抗体药物研发领域
Eureka:E轮融资4500万美元,华人科学家继续发力抗体药物研发领域近日,动脉网获悉,美国生物技术公司Eureka Therapeutics宣布完成4500万美元E轮融资。本轮
近日,动脉网获悉,美国生物技术公司Eureka Therapeutics宣布完成4500万美元E轮融资。本轮融资由Lyell Immunopharma领投,并有一个由新老投资者组成的财团参与。
一路走来,Eureka Therapeutics融资频率并不高。其融资金额与生物技术领域创新公司中的个别新起之秀获得的上亿美元融资相比,甚至不算多。但是Eureka自2006年创立始,已走过了14个年头。成立至今,每次融资都是稳打稳妥,目前已经进行至E轮。
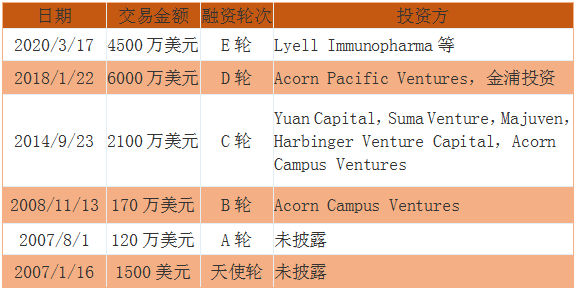
Eureka Therapeutics融资历史
在生物技术领域,一项新的技术若无超硬实力与超强团队孵化,或缺乏了研究平台技术所需的强大资金支持,想要长期走下去,很难。
那么Eureka Therapeutics又是怎样以一个“稳重者”的姿态在生物创新领域行走,获得各大投资公司的青睐?
华人科学家领导的团队
Eureka Therapeutics Inc.成立于2006年2月,总部坐落在美国生物医药产业最活跃的旧金山湾区,是一家具备雄厚新药研发实力、拥有多项国际专利和自主知识产权的高科技生物公司。该公司主要致力于针对癌症的新一代抗体免疫治疗。
它还有一个现位于北京清华科技园的全资子公司:优瑞科(北京)生物技术有限公司。该公司成立于2007年4月,目前主营方向是运用自主研发的ALPHATM全人源噬菌体抗体库技术平台筛选性质优良的抗体药物候选者。
华人科学家刘诚是Eureka Therapeutics Inc.的创始人兼首席执行官。他拥有北京大学以及加州大学伯克利分校的博士学位,在生物学研究和药物发现方面拥有20多年的经验,在癌症治疗性抗体的发现和开发方面具有广泛的经验和知识。

创始人&CEO 刘诚
图片来源:Eureka Therapeutics官网
在创立Eureka之前,Liu博士曾在Chiron(现已成为诺华的一部分)的抗体药物发现计划中担任首席科学家。他在美国和欧洲申请了18项发明专利,还于2004年至2005年担任SAPA-West的总裁,1998-2007年担任其执行委员会和咨询委员会的主席。
研发“不可达到”疗法
作为一家抗体药物研发商,Eureka Therapeutics致力于改善T细胞疗法的安全性,开发适用于恶性血液疾病和实体瘤的T细胞疗法。
同时,Eureka Therapeutics公司拥有多项国际专利和自主知识产权的核心技术,如大容量的全人源噬菌体抗体库ALPHATM、抗体ADCC增强技术等。
其核心技术围绕其专有的ARTEMIS T细胞受体平台和噬菌体ALPHATM展示文库,通过MHC I类复合物发现和设计针对细胞内靶标的人源抗体。
Eureka Therapeutics的ALPHATM(Adaptive Library Panning for Human Antibody) 全人源噬菌体抗体库技术平台库容量大,天然库和半合成库的总库容量达到了8.86*1010 ;淘选技术灵活多样:因其以独立亚库的形式保存,可据项目特点选用不同来源、不同CDR特性的亚库,以达到最佳淘选效果;候选克隆鉴定技术专业高效,抗体来源也十分丰富:包括健康人脾脏、外周血;特殊疾病(如:自身免疫病)病人的外周血等。
ALPHATM是一个多样性丰富的全人源噬菌体抗体库,是一个专门为开发全人源抗体药物设计的综合性技术平台,而Eureka是世界上第一家拥有此项技术的公司。
Eureka的技术疗法曾被认为是不可达到的。因为传统T细胞疗法主要都是以T细胞受体识别细胞外部蛋白从而实现靶向攻击致病蛋白。然而癌细胞的致病蛋白却往往是胞内蛋白,很难被识别出来。
Eureka Therapeutics专有的技术平台ALPHATM旨在发现可通过MHC肽复合物识别细胞内蛋白质片段的抗体,从而为针对以前无法接近的潜在靶标进行免疫治疗开辟道路。这些抗体可以有效地到达癌细胞内部以识别与癌症相关的蛋白质,然后动员免疫系统进行攻击。
原理如下:细胞内的蛋白质在正常细胞功能期间分解时,这些蛋白质(肽)的片段会被MHC(主要组织相容性复合物)分子带到细胞表面。当T细胞(犹如免疫系统“皇家护卫队”的一个分支)将这些片段识别为异常时,它们会杀死患病的细胞,从而达到治疗疾病的目的。
共寻抗体,Eureka终遇“知音”
科研之路枯燥寂寞,但充满了想象空间。科学家们正是凭借着自己所憧憬、所构筑的理想世界,用一腔热血在未知的神秘世界进行探索。这是一场理想与现实的较量与权衡。当理想的实现度高,那么理想就值得义无反顾的坚持。在此途中,科学家们会找到真正志同道合的朋友。
Memorial Sloan-Kettering癌症中心(以下简称MSKCC)就是其中之一。MSKCC发现,在多种白血病和实体肿瘤中有一种蛋白抗原——Wilms tumor 1(即WT1),这种蛋白会过量表达,但由于它是一种细胞内的转录因子,待它表达成蛋白质后还是在细胞内。而通常抗体又不能直接作用于胞内蛋白,小分子药物通常也无法调节涉及转录因子的蛋白质间的相互作用。
但是,WT1的来源含有9个氨基酸残基的多肽,可用来激活针对一些类型的WT1阳性肿瘤细胞的T细胞免疫反应。这些多肽被一类称为HLA-A 0201的分子处理并以HLA/peptide复合物的形式呈递在细胞表面。随之,T细胞受体就可通过对这些呈递了HLA/peptide复合物的癌细胞进行攻击,引发T细胞免疫反应。
在当时,应用抗体或小分子药物治疗WT1阳性癌症的研究集中在疫苗开发和T细胞疗法两个方面。疫苗开发是当时的主流。有好几家公司针对WT1阳性癌症开发的免疫疗法已进入临床实验阶段。
本来当时的MSKCC也想开发一个针对癌症的疫苗(若当时的MSKCC研究的重心贯注于此,可能也就没有如今两家公司携手研究的突破性成果了)。但是,MSKCC发现,所有接受免疫疗法临床试验的人群都是处于缓解期或是病情较轻的患者,而非那些病情严重(more active disease)的患者。鉴于WT1多肽-HLA复合物也存在于细胞表面,需要重新评估使用治疗性单克隆抗体识别WT1阳性细胞的可能性。
MSKCC的Scheinberg教授说,“疫苗的方法最有可能适用于那些经过其它方法治疗后残存肿瘤组织难以检测到白血病或肿瘤。而抗体可以用来治疗活跃肿瘤,而且比使用患者特异的活性T细胞疗法要简便得多。”
基于对此种治疗方式的大胆构想与其“光辉”的应用前景,MSCKK团队在2010年与Eureka公司开始了合作,以寻找能直接识别HLA/WT1衍生肽复合物的单克隆抗体。
突破性成果——单克隆抗体ESK1
2013年3月4日,双方研究人员发现了一种独特的单克隆抗体ESK1,可以有效地到达癌细胞内部,靶向驻留在细胞内部的WT1蛋白质(在一系列白血病和其他癌症,如骨髓瘤、乳腺癌、卵巢癌和结肠直肠癌中会过量表达,又由于在健康的细胞中很少发现它,因此靶向它的药物产生副作用的可能性较小)。
Eureka Therapeutics总裁兼首席执行官刘诚博士说,“ ESK1代表了人类单克隆抗体治疗领域的典范变革。这项研究表明,人抗体治疗不再局限于靶向癌细胞外部存在的蛋白质,而是现在可以靶向癌细胞本身中的蛋白质。”
在关于ESK1的研究中,研究人员表明,单独的ESK1能够识别WT1肽并杀死试管以及两种不同类型人类白血病的小鼠模型中的癌细胞。在准备对患者进行ESK1检验之前,必须在实验室中进行其他研究。但是,由于单克隆抗体的设计完全是人类的,就加快了将药物运到临床所需的时间。
当时,刘诚博士和MSKCC的Scheinberg博士都认为治疗性的单克隆抗体具有不可替代的实用性,因为它为患者提供了一种潜在的治疗活跃肿瘤的方法。
大阪大学药学院功能性诊断科学系教授Haruo Sugiyama也是此领域的专家。他当时对ESK1充满期待,因为他认为,想要治愈白血病,必须要彻底杀死肿瘤干细胞;如果ESK1结合细胞上的WT1衍生肽-HLA复合物的方式与WT1特异识别淋巴细胞足够相似,应该可以杀死白血病干细胞。
该抗体是在Memorial Sloan-Kettering和Eureka Therapeutics之间共同开发的,两家公司已共同申请了专利保护。
Eureka Therapeutics总裁兼首席执行官刘诚说:“这种合作关系凸显了学术界、生物技术公司和制药公司如何共同为患者提供创新的癌症治疗方法。ESK1的成功将改变抗体疗法领域。这将验证抗细胞内抗原的单克隆抗体的使用,而在从前,这被认为是‘不可治疗'的靶标。”
在这条向前行进的道路上,Eureka Therapeutics找到了越来越多的“知音”。

管道合作(伙伴关系)
首选肝癌作为突破,CAR-T攻克实体瘤未来可期
肝癌死亡率居恶性肿瘤死亡率第二位,全球每年大约有60万人死于肝癌。过去16年,美国肝癌死亡率上升了43%,每年大约有3.15万新病例。这也是Eureka Therapeutics公司的创始人兼CEO刘诚博士团队首选肝癌作为突破的原因。
由于Eureka和MSKCC共同发现的单克隆抗体ESK1一方面作为抗体生物药,在肿瘤动物模型中被证实具有令人满意的免疫治疗效果,而同时可以作为专一性识别肿瘤细胞的单链抗体,应用到CAR-T治疗上。
而新设计的CAR-T细胞能够分泌一种简化版的免疫检查点阻断抗体。这种抗体的功能与已经获得FDA批准的nivolumab和pembrolizumab非常类似。它们能够与PD-1蛋白结合,通过阻断其“刹车”功能,让CAR-T细胞和肿瘤周围的免疫细胞更有效地对抗癌症。

专有Artemis AbTCR管道
2018年7月19日,Eureka与西安交通大学第一附属医院联合开启结构优化的ET019002-T细胞治疗难治/复发性B淋巴细胞恶性肿瘤的前瞻性临床研究。前期的动物实验以及人体预实验已经显示了ET019002-T细胞治疗恶性B淋巴细胞肿瘤的有效性和安全性。
2019年8月6日,Eureka在美国启动名为ET140202 Artemis的T细胞疗法治疗肝癌的1/2期临床试验。旨在检验该疗法治疗晚期肝细胞癌(HCC)患者的安全性和疗效。
2018年9月5日,Eureka Therapeutics在世界肿瘤细胞免疫治疗峰会发布了针对甲胎蛋白阳性晚期肝细胞肝癌(一种最普遍的肝癌)患者的ET140202 ARTEMIS? T细胞免疫疗法临床研究的初步安全性和疗效数据:ET140202导致6例可评估患者中1例完全肿瘤消退,2例部分肿瘤消退。
刘诚博士在峰会上表示,“将T细胞免疫疗法与T细胞受体模拟抗体相结合,以癌细胞内源的特异靶点为目标来攻击癌细胞,是一种新颖且潜力巨大的治疗方法。Eureka ET140202在治疗甲胎蛋白阳性肝癌时的安全性数据和初步观察疗效令人鼓舞,这种方法可能成为一种治疗实体肿瘤的有效手段,尤其是针对肝癌这种现在急需有效治疗方法的癌症。”
2019年3月27日,Eureka宣布GPRC5D是合理设计CAR-T细胞免疫治疗多发性骨髓瘤的靶点。研究进一步表明,在BCMA抗原丢失导致的肿瘤复发模型中,GPRC5D靶向的CAR-T疗法可以克服肿瘤逃逸。
2018年12月3日,Eureka与Celgene公司联合发布了JCARH125概念验证试验的初步临床数据。JCARH125是由Celgene旗下公司Juno Therapeutics开发的靶向BCMA治疗复发/难治性多发性骨髓瘤的CAR-T细胞疗法。
2020年3月17日,Eureka Therapeutics宣布获得第E轮融资,还与Lyell进行了战略合作,欲开发针对多种癌症类型中几个未公开的实体肿瘤靶点的治疗方法。
Eureka公司表示,将利用E轮融资的收益,推进其专有的TCR-mimic和抗体- TCR ARTEMIS?项目,包括Eureka的抗AFP ARTEMIS?I/II期临床试验,继续推进对于肝癌(HCC)的研究。
作者:陈宣合
-
解构Genmab:收入增长77.4%,丹麦这家生物上市公司在如何推进抗体药物研发?2020-03-02
-
钟南山宣布好消息:国家批准两个新冠病毒抗体试剂盒2020-02-24
-
浙江第一批新冠肺炎疫苗已产生抗体,近期将开展动物实验2020-02-24
-
新冠病毒治愈患者抗体有效 中国生物治疗性新冠特免血浆制品投入临床2020-02-14
-
全国现假阴性病例,抗体诊断试剂已近临床试验阶段2020-02-11
-
三生国健申报科创板,已有两款抗体药物上市2019-11-04
-
灵北制药以19.5亿美元收购生物制药公司Alder,引进偏头痛抗体药物2019-09-20
-
LifeArc向Kymab注资3000万美元,研发全人源单克隆抗体2019-07-09
-
岸迈生物完成7400万美元B轮融资,用于发展和推进公司新型双特异性抗体的临床开发2019-06-07